ゼーゲル(式)ついて
釉薬のことをどんどん勉強していくと必ず「ゼーゲル式」という壁?にぶつかります。
趣味で陶芸をしていて、市販の釉薬を使っている分にはあまり関係ないことかもしれませんが、
もう一歩進んで、自分だけの釉薬を造ろうと考えている人には避けて通れないことだと思いますので解説したいと思います。

| 錐番号 | 温度C |
|---|
| SK 05a | 1000 |
| SK 04a | 1020 |
| SK 03a | 1040 |
| SK 02a | 1060 |
| SK 01a | 1080 |
| SK 1a | 1100 |
| SK 2a | 1120 |
| SK 3a | 1140 |
| SK 4a | 1160 |
| SK 5a | 1180 |
| SK 6a | 1200 |
| SK 7 | 1230 |
| SK 8 | 1250 |
| SK 9 | 1280 |
| SK 10 | 1300 |
ドイツ人の科学者ゼーゲル(Hermann August Seger:1839-1893)は明礬工場の技術を担当したり、
窯業雑誌の編集者をして化学的知識を貯え、やがてベルリン王立製陶所の研究所所長となりました。
そこで系統的な熔融(物の熔け易さ)性に関する研究をし、その結果「ゼーゲル錐(コーン)」
が発表されることとなりました。ゼーゲル錐は、窯内の温度を測るための三角錐状の用具でその曲がり具合で温度を判断します。さらに素地と釉の適合性の研究において釉式「ゼーゲル式」が生まれ、
今なお釉薬の計算にはこの式が使われているのです。ですから釉薬を勉強しようとするとどうしても化学式を、
そして計算にゼーゲル式を勉強せざるをえなくなるのです。
ゼーゲル式でどんなことがわかるのか?
1.釉薬の範囲を示す
素地及び釉が化学組成においてどの範囲まで変えられるかを示すことが出来る。
つまり、釉薬の調合を変えようとした場合、釉式から具体的に数字で何をどれだけ加えるなり、
減らすべきかを計算できるわけです。とはいうものの陶芸家の方々はこれを長い経験を通して
体得しているので役に立たないと言われる方もあるかと思います。この釉式はあくまで量産する、
つまり工業向けに作られたものだからです。
2.調合を計算する
文献にゼーゲル式の形で調合が載っていることがあります。その式から調合を計算することが出来ます。
たとえそれが英語で書かれたものであっても、その地にしかない原料を使っていたとしても
代わりに手に入る原料を使ってほぼ同じ釉を造ることが出来ます。
3.系統的に把握
系統的に釉薬を把握し最短で理解することが出来る。もちろん実際にいろいろテストは必要ですが。
具体的にゼーゲル式とは次のようなものです。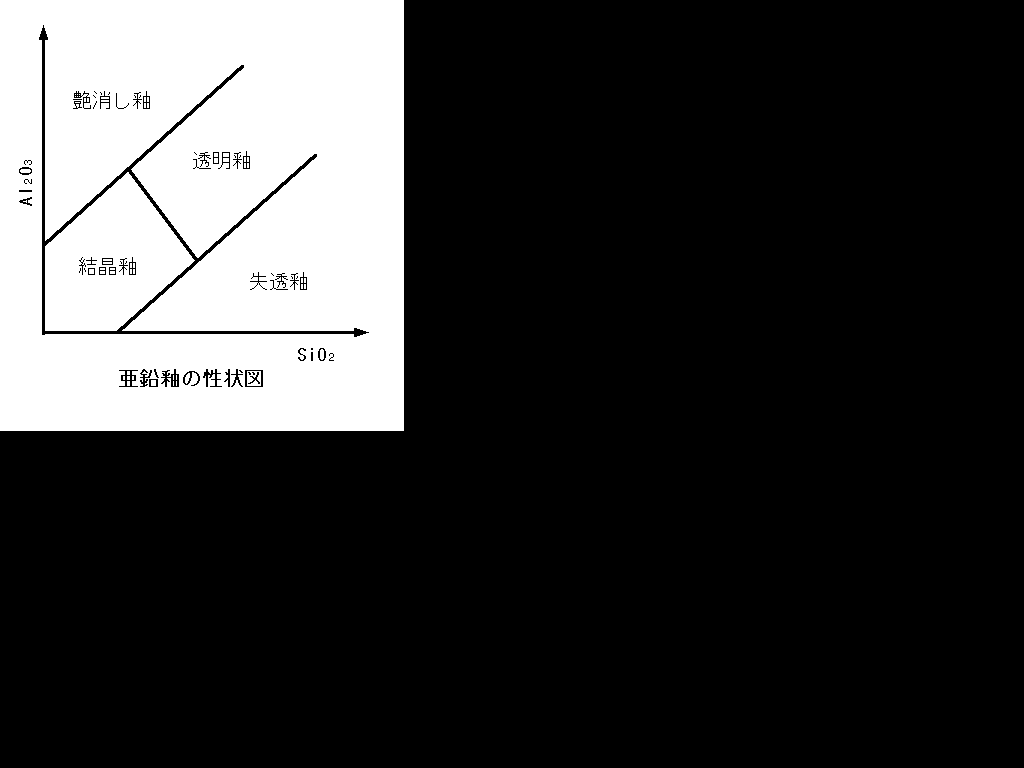
0.2 KNaO
0.5 CaO ・ 0.4 Al2O3・4.5 Si2O
0.3 MgO
<解説>
上のゼーゲル式で 0.2, 0.5, 0.3, 0.4, 4.5 と書いてある数字の単位はモル(mol)です。
化学の時間に習ったとは思いますが、まあ分子の数と思って下さい。
KNaO は K2O(カリ)と Na2O(ソーダ)を合算して簡略化したもの
CaO は石灰(酸化カルシウム)
MgO はマグネシア(酸化マグネシウム)
Al2O3 はアルミナ(酸化アルミニウム)
Si2O は珪酸(シリカ)です。
そして、ポイントは KNaO と CaO と MgO が左側に書いてあり、その数字の合計は 0.2 + 0.5 + 0.3 = 1.0で 1.0 であること。
Al2O3 は真ん中に書いてあり、釉薬の場合 0.1 から 1.0 モルの範囲がほとんどであること。
Si2O は右端に書き、 1.0 から 10.0 モル位の値になることです。
左端は塩基成分で Na2O, K2O, CaO, MgO, BaO, ZnO, PbO, Li2O, SrO などで、熔けやすくする成分からなります。
この塩基成分の種類と比率から熔けやすさや貫入の入りやすさ、発色具合などを判断します。
塩基成分の合計が 1.0 とするのがゼーゲル式ですから、当然 Si2O のモル数が小さくなれば、熔けやすい成分の方が多く、低い温度で熔ける釉となります。
真ん中は中性成分、右端は酸性成分で両成分の比率により、艶消し、透明、乳白などを判断します。
例えば一般的な磁器釉の場合、 Al2O3 と Si2O のモル比が1/7から1/10のときに光沢透明釉になり、それ以外では艶消しとなる。
亜鉛の入った釉ではモル比が小さくなると乳濁(乳白)しやすい。(性状図参照)
このほか CuO などを塩基成分に、Fe2O3 などを中性成分に TiO2 などを
酸性成分に入れたりすることもありますが着色成分は別にして、後入れという形の方が一般的のようです。
実際には各原料の化学的分析値からmol数を計算し、
塩基成分を1にしてゼーゲル式を求めます。
あるいは、その逆を行いますが、詳しくは「釉調合の基本」加藤悦三著、「陶磁器釉の科学」高嶋廣夫著などを参考にしてください。
HOME

